Предложен новый подход к лечению травм спинного мозга на основе блокады цитокиновых рецепторов
Предложен новый подход к лечению травм спинного мозга на основе блокады цитокиновых рецепторов
Группа исследователей из ГНЦ Институт биоорганической химии им. академиков М.М. Шемякина и Ю.А. Овчинникова РАН и НИИ нейрохирургии им. Н.Н. Бурденко представила революционный подход к лечению травм спинного мозга. Результаты исследования опубликованы в Advanced Science.
Травмы спинного мозга (ТСМ) — одна из наиболее серьёзных медицинских проблем современности. После первичной механической травмы развивается вторичное повреждение тканей, продолжающееся несколько недель и приводящее к формированию глиального рубца, который препятствует восстановлению проводимости нервных волокон. Несмотря на почти полувековую историю экспериментальных исследований, эффективные методы лечения ТСМ до сих пор крайне ограничены.
Для моделирования ТСМ у пациентов исследователи выбрали уникальный подход: они изучали пациентов, подвергавшихся хирургическому удалению интрамедуллярных опухолей спинного мозга. Этот выбор был обоснован несколькими факторами: стандартизированная хирургическая техника, возможность корреляции размера опухоли с амплитудой цитокинового ответа и, что критически важно, возможность синхронизированного забора образцов плазмы и цереброспинальной жидкости.
Исследовательская группа провела комплексное изучение динамики цитокинового и хемокинового ответа при ТСМ у людей и лабораторных животных. Были проанализированы образцы плазмы крови, цереброспинальной жидкости и тканей спинного мозга в восьми временных точках и определены концентрации цитокинов и хемокинов.
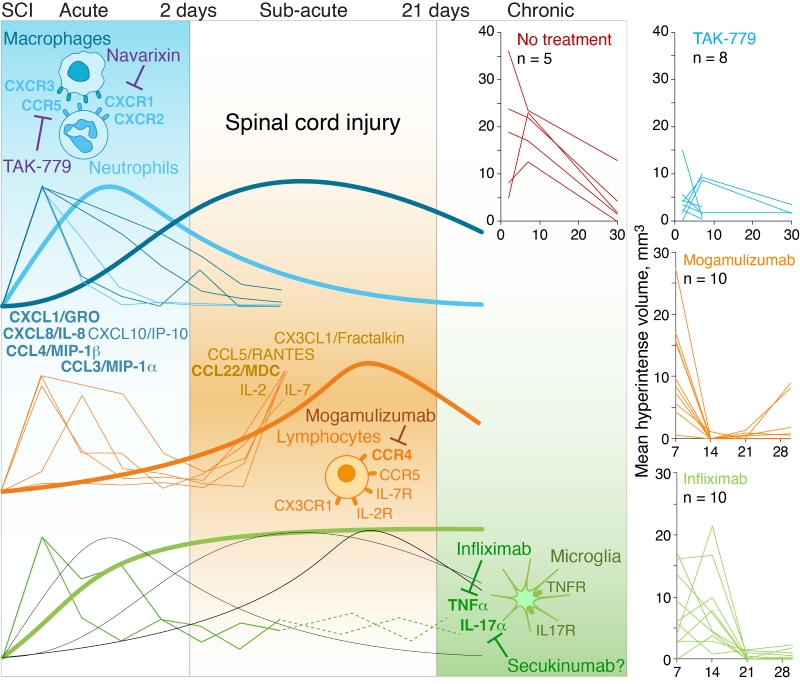
Ключевое открытие исследования — выявление трёх различных фаз воспалительного ответа при ТСМ:
- Острая фаза (0—48 часов): характеризуется массивным «цитокиновым штормом» в цереброспинальной жидкости, главным образом обусловленным повышением уровня нейтрофильного хемоаттрактанта CXCL1 (в 1000 раз выше базального уровня у человека), а также IL-6, IL-8, CCL2-5 и G-CSF (в 40-600 раз). У крыс наблюдалось 10-200-кратное повышение CXCL1, IL-6, CCL2, CCL3, CCL5 и G-CSF.
- Подострая фаза (3-14 дней): отмечается постепенное снижение большинства провоспалительных медиаторов, но увеличение уровней IL-2, IL-7, CCL22 и CX3CL1 в цереброспинальной жидкости человека к седьмому дню после травмы, что указывает на рекрутирование Т-клеток в центральную нервную систему.
- Хроническая фаза: TNFα и IL-17α персистируют в ЦНС на протяжении недель после травмы, поддерживая хроническое воспаление.
- TAK-779 (низкомолекулярный антагонист CCR5/CXCR3) и MK-7123/Навариксин (антагонист CXCR1/2) продемонстрировали выраженный эффект в острой фазе ТСМ, значительно уменьшая воспаление и отёк спинного мозга в первую неделю после травмы.
- Могамулизумаб (моноклональное антитело против CCR4, одобренное для лечения кожных Т-клеточных лимфом) оказался наиболее эффективным в предотвращении вторичного воспаления в поврежденной области в подострой фазе (14-21 день после травмы). Препарат значительно уменьшал объем гиперинтенсивных областей на МРТ, минимизировал формирование кист и способствовал формированию более компактного глиального рубца.
- Инфликсимаб (анти-TNF антитело) также показал положительный эффект, уменьшая объем гипоинтенсивных повреждений в течение первых трех недель и способствуя более глубокому проникновению GFAP-позитивных клеток в дефектную зону.
Важно отметить, что все протестированные препараты, за исключением соединения TAK- 779, уже одобрены для клинического применения или проходят клинические испытания.
«Наше исследование демонстрирует принципиальную возможность репозиционирования существующих препаратов для лечения травм спинного мозга. Критически важно, что эффективность терапии зависит от времени начала лечения. Блокада хемокиновых рецепторов наиболее эффективна в острой фазе, в то время как терапия моноклональными антителами, такими как могамулизумаб, может быть начата даже через 1-2 недели после травмы, что открывает новые возможности для пациентов, не получивших своевременную медицинскую помощь. Описанный подход не ограничивается только травматическими повреждениями спинного мозга, он потенциально применим и в реабилитации после плановых нейрохирургических вмешательств», — прокомментировал первый автор работы профессор РАН Алексей Белогуров.
Исследование выполнено при поддержке Биоресурсной коллекции SPF-лабораторных грызунов для фундаментальных, биомедицинских и фармакологических исследований #075-15-2025-486.
Источник: ИБХ РАН.